La Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) actualizó este martes 30 de julio su alerta sanitaria sobre la comercialización irregular del producto BOTOX 100 U (Toxina Botulínica Tipo A), tras identificar nuevos casos de falsificación en territorio nacional. La alerta complementa los avisos emitidos previamente los días 30 de mayo de 2023 y 27 de mayo de 2024.
De acuerdo con la información presentada por la empresa importadora y distribuidora AbbVie Farmacéuticos, SA de CV, se detectó la venta ilegal del producto en redes sociales, en presentaciones que muestran irregularidades.
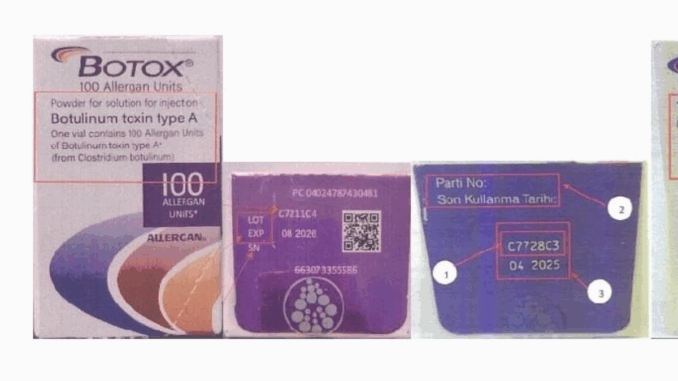
Entre los lotes identificados se encuentran los números C7211C4 con fecha de caducidad agosto de 2026, y C7728C3 con fecha de abril de 2025. Ambos fueron reportados como no comercializados por el distribuidor autorizado. Además, los empaques primario y secundario de estos productos están etiquetados en un idioma diferente al español y no cuentan con registro sanitario ante la COFEPRIS.

Asimismo, una agencia internacional notificó a la autoridad sanitaria mexicana sobre un tercer lote falsificado, correspondiente al producto BOTOX 150 U con número C3709C3 y fecha de caducidad diciembre de 2025. Este número de lote ya había sido reportado en 2023 en un caso previo de falsificación del producto BOTOX 100 U, pero con una fecha de caducidad diferente, lo que sugiere una posible reutilización del lote y alteraciones deliberadas de su caducidad.
COFEPRIS reiteró que la compra de medicamentos en redes sociales o sitios no regulados incrementa significativamente el riesgo de adquirir productos falsificados, contaminados, alterados o introducidos al país de forma ilegal. Estos productos representan un riesgo para la salud de la población, ya que no se puede garantizar su calidad, eficacia o seguridad.
La autoridad sanitaria recordó que BOTOX es un medicamento de uso controlado que requiere prescripción médica, conforme al artículo 226 de la Ley General de Salud. Su uso indiscriminado y sin supervisión médica puede ocasionar reacciones adversas graves.
Ante esta situación, COFEPRIS pidió a la población evitar adquirir medicamentos que presenten etiquetado en idiomas distintos al español o que no cuenten con registro sanitario. También se recomendó realizar una inspección visual del empaque para verificar que los datos como número de lote y fecha de caducidad coinciden y no presentan anomalías.
En caso de haber adquirido o utilizado un producto con las características descritas, la población puede reportarlo a través del correo farmacovigilancia@cofepris.gob.mx o mediante el sitio oficial de la institución. También se invita a realizar denuncias sanitarias si se detecta la venta de estos productos en internet o redes sociales.
A los distribuidores y farmacias se les exhortó a no adquirir ni comercializar productos que no cumplan con los requisitos legales y sanitarios establecidos, y a verificar que sus proveedores estén debidamente autorizados por COFEPRIS y cuenten con la documentación que respalde la legalidad del producto.




Be the first to comment