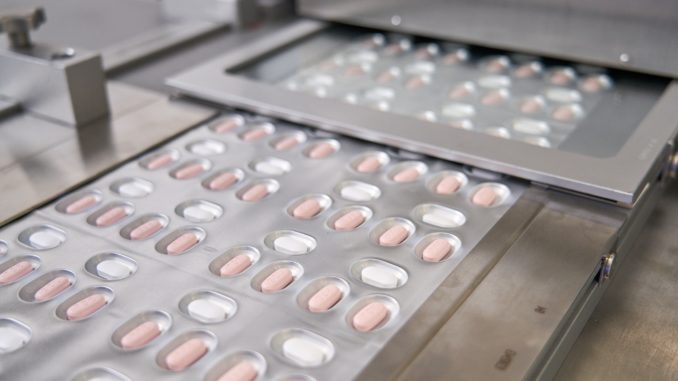
A través de un comunicado, la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) informo que autorizó el uso del medicamento Paxlovid de la farmacéutica Pfizer para el tratamiento de la COVID-19. Siendo México el primer país de América Latina en aprobar esta pastilla.
Al igual que el Monulpiravir de Merck, la pastilla Paxlovid no se podrá tomar sin prescripción médica pues se autorizó para uso de emergencia y de manera controlada.
Con el objetivo de reducir el riesgo de hospitalización por Coronavirus, “el medicamento que combina nirmatrelvir y ritonavir en presentación tabletas, será destinado para atender pacientes adultos con COVID-19 leve o moderado y con riesgo de complicaciones.”
Cabe señalar que los componentes de Paxlovid contribuyen a reducir hasta un 88% la tasa de hospitalización y mortalidad a causa del SARS-CoV-2. El fármaco de Pfizer contiene nirmatrelvir y ritonavir.
El nirmatrelvir es el encargado de bloquear la replicación del virus mediante la inhibición de la enzima proteasa, el ritonavir tiene la función de aumentar la duración de la efectividad, evitando que el hígado humano deseche el retroviral.
Por su parte, Alejandro Svarch Pérez, titular de la Cofepris, celebró que este tratamiento permita evitar que se agraven los contagios por COVID-19: “Estos tratamientos serán clave para reducir las hospitalizaciones en México, por lo que celebramos ser el primer país de América Latina en autorizar su uso de emergencia”.
La Cofepris señaló que se sumó a un llamado internacional para informar a la población que el Paxlovid no sustituirá la campaña de inmunización contra COVID-19, reiterando que no se use sin prescripción profesional en la medicina.
Asimismo, la Cofepris hizo un llamado para que la población haga una denuncia sanitaria en caso de encontrar a la venta la pastilla de Pfizer contra COVID-19, “ya que su consumo irregular constituye un riesgo a la salud por ser de dudosa procedencia”.
Fuente: Infobae






Be the first to comment